(Beschrijving in ‘lekentaal’)
Inleiding:
Trafinib als nieuwe behandeling voor het multipel myeloom en de Ziekte van Waldenström
Ondanks de ontwikkeling van nieuwe behandelingen blijven het multipel myeloom en de Ziekte van Waldenström ernstige ziekten, waarvoor tot nu toe geen curatieve behandelingen bestaan. Aanvullende behandelingen zijn daarom dringend noodzakelijk. In dit project willen we onderzoeken of en hoe een nieuwe en innovatieve behandeling gericht op het ontstekingseiwit CD40, genaamd Trafinib, het beloop van multipel myeloom en de Ziekte van Waldenström zou kunnen beïnvloeden.
Eerder onderzoek heeft aangetoond dat CD40 zorgt voor activatie en celdeling van multipel myeloom en Waldenström cellen. Daarnaast heeft het eiwit een rol in de ontwikkeling van therapieresistentie van de kankercellen. Specifieke remming van CD40 is dan ook een potentiele behandelstrategie voor het multipel myeloom en de Ziekte van Waldenström. Omdat CD40 ook een belangrijke functie heeft in andere celtypen is algehele remming van CD40, bijvoorbeeld met een antilichaam, ongeschikt omdat dit ernstige bijwerkingen geeft doordat het aangeboren immuunsysteem wordt geremd.
In dit project willen we onderzoeken of een meer specifieke remming van CD40, welke geen effecten heeft op het aangeboren immuunsysteem, een potentiële behandeling is voor het multipel myeloom en de Ziekte van Waldenström. Deze nieuwe remmers hebben wij eerder ontwikkeld als behandeling voor ontstekingsziekten en worden Trafinibs genoemd.
Doelstelling:
In dit project willen we in cellijnen onderzoeken wat de effecten zijn van Trafinib- gemedieerde remming van CD40 gedreven activatie van multipel myeloom en Waldenström cellen, om zodoende te evalueren of Trafinib een potentiele nieuwe therapie voor het multipel myeloom en de Ziekte van Waldenström kan worden.
Uitvoering:
Om de effectiviteit van Trafinibs als potentiële behandeling te onderzoeken zullen we gebruik maken multipel myeloom cellijnen en Waldenström cellijnen. Deze worden behandeld met Trafinibs en vervolgens zullen we de activatie, celdeling, apoptose en productie van bijvoorbeeld ontstekingsstoffen uitvoerig in kaart brengen. Ook zullen we de moleculaire effecten van Trafinibs op deze cellen ophelderen. Op basis van deze uitgebreide experimenten ontstaat een compleet beeld van de therapeutische potentie van Trafinibs en verwachten we de vervolgstudies te kunnen ontwerpen die nodig zijn om Trafinibs verder te ontwikkelen als nieuwe behandeling voor patiënten met een multipel myeloom of de Ziekte van Waldeström. Omdat trafinibs al worden ontwikkeld voor andere ziekten waardoor veiligheids resultaten van behandeling met deze middelen beschikbaar komen, zal een eventuele vertaling van de onderzoeksresultaten in het laboratorium naar een klinische studie relatief snel kunnen gaan.
Uitgebreide beschrijving project
Introductie
Ondanks de ontwikkeling van nieuwe behandelingen blijven het multipel myeloom (MM) en het lymfoplasmacytair lymfoom (LPL; Ziekte van Waldenström) ernstige hemato- oncologische ziekten, waarvoor tot nu toe geen curatieve opties bestaan. Aanvullende therapeutische strategieën zijn derhalve dringend noodzakelijk. In dit project willen we de therapeutische waarde van een nieuwe ‘targeted therapy’, genaamd Trafinib, onderzoeken.
CD40: een essentieel immune checkpoint eiwit in MM en LPL
Het immuun checkpoint eiwit CD40 heeft een belangrijke functie in de regulatie van zowel goed- als kwaadaardige B-cellen en plasmacellen. Zo is aangetoond dat activatie van CD40 in MM en LPL cellen resulteert in activatie, proliferatie en therapieresistentie (Fig. 1A). In LPL cellen induceert CD40 activatie eveneens toename van IgM productie. Specifieke remming van CD40 is derhalve een veelbelovende therapeutische strategie voor MM en LPL.
Trafinib: een nieuwe CD40-targeted therapie in MM en LPL?
Omdat het eiwit CD40 ook een belangrijke functie heeft in andere celtypen, zoals monocyten, is remming van CD40 d.m.v. monoclonale antilichamen een ongeschikte strategie voor de behandeling MM en LPL, aangezien dit zou kunnen leiden tot potentieel levensbedreigende bijwerkingen, waaronder suppressie onderdrukking van het aangeboren afweersysteem. Een meer specifieke remming van de door CD40 geïnduceerde intracellulaire signaleringscascade kan deze bijwerkingen voorkomen.
Na activatie van CD40 worden er intracellulaire adaptoreiwitten uit de tumor necrosis factor receptor-associated factors (TRAF) familie gerekruteerd, welke zorgen voor de initiatie van signaaltransductiecascades en cellulaire activatie. In goedaardige B cellen, MM en LPL cellen rekruteert CD40 de eiwitten TRAF2/3/5, terwijl in monocyten en macrofagen TRAF6 wordt gerekruteerd (Fig. 1B). Inhibitie van de interactie tussen CD40 en TRAF2/3/5 is dus een potente strategie om CD40-gemedieerde activatie van MM en LPL cellen te remmen, zonder de rol van CD40-TRAF6 gemedieerde activatie van het aangeboren afweersysteem te beïnvloeden. Recent hebben wij een small molecule
inhibitor ontwikkeld welke de interactie tussen CD40- en TRAF2/3/5 remt (Fig. 1C).
Wij hebben aangetoond dat deze inhibitor, genaamd Trafinib, B cel activatie en proliferatie remt, alsmede de productie van immuunglobulines door plasmacellen. In dit project willen we onderzoeken of Trafinib ook in staat is CD40-gemedieerde activatie van MM en LPL cellen te remmen en daarmee een potentiele nieuwe ‘targeted therapy’ voor het multipel myeloom en het lymfoplasmacytair lymfoom kan worden.
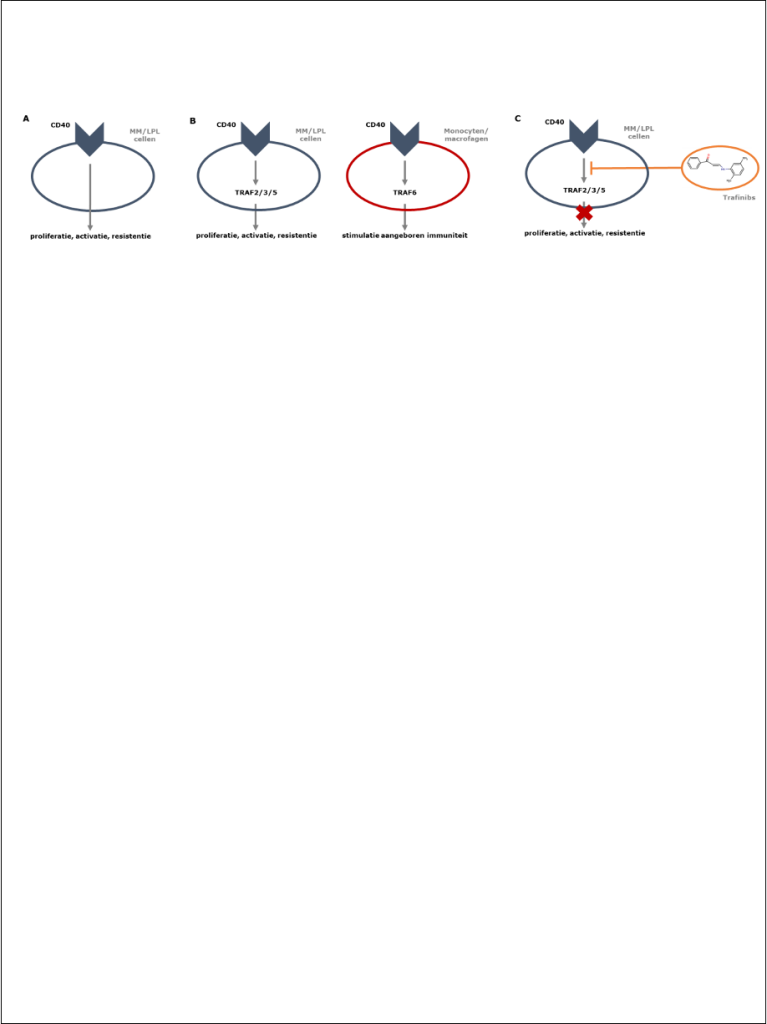
Figuur 1. Trafinib gemedieerde remming van CD40-TRAF2/3/5 interacties is een potentiele ‘targeted therapy’ voor MM en LPL. A) Activatie van het membraan eiwit CD40 resulteert in activatie van MM en LPL cellen. B) CD40 gemedieerde activatie van MM en LPL cellen verloopt via TRAF2/3/5 interacties, terwijl dit in myeloïde cellen via TRAF6 verloopt. C) Trafinibs zijn ‘small molecule inhibitors’ die de interactie tussen CD40 en TRAF2/3/5 remmen.
Onderzoeksstrategie
Om de effectiviteit van Trafinib als potentiële therapeutische strategie te onderzoeken zullen we gebruik maken van goed gekarakteriseerde MM cellijnen (o.a. L363, LME1, OPM1, WPC1) en LPL cellijnen (BCWM1, MWCL1, RPCI-WM1). Er worden 2 strategieën toegepast om de cellijnen te activeren: 1) farmacologische activatie d.m.v. agonistische CD40 antilichamen; 2) activatie d.m.v. co-cultuur met van fibroblasten die CD154 (de activerende ligand van CD40) tot expressie brengen. Cellijnen zullen gedurende verschillende tijdsperioden worden behandeld met Trafinib, tevens zullen er verschillende concentraties Trafinib worden toegepast om zodoende de beste in vitro behandelstrategie te identificeren. Vervolgens zullen de hieronder benoemde kenmerken worden geanalyseerd in met Trafinib of het oplosmiddel behandelde cellijnen:
– Celcyclus status (propidium iode (PI) flow cytometry (FACS))
– Proliferatie (CFSE-FACS; BrdU incorporatie assay; expressie van celcyclus genen (o.a. cyclines, cyclincine-dependent kinases) d.m.v. qPCR)
– Apoptose (Annexin V FACS; expressie van apoptose regulators (o.a. BCL2, BCL6, BAX, p21, p53) d.m.v. qPCR)
– Expressie van activatie markers en immune checkpoint eiwitten (o.a. CD80/86, CD18, CD11a, CD54, CD70 d.m.v. FACS, specifieke markers verschillen per cellijn)
– Expressie van cytokines en immuunglobulines (o.a. IL1β/6/8/10, TNF, IgM, IgG, IgA
d.m.v. FACS, qPCR, ELISA, specifieke eiwitten verschillen per cellijn)
– Expressie van drug-resistance eiwitten (o.a. multidrug resistant protein (MRP)1, multidrug resistance (MDR)1/2, interferon regulatory factor 4 d.m.v. qPCR, specifieke eiwitten verschillen per cellijn)
Om de moleculaire effecten van Trafinib verder in kaart te brengen zal RNA-sequencing worden uitgevoerd op MM en LPL cellijnen, gevolgd door pathway/network analysis (Ingenuity-Pathway-Analysis) en gerichte validaties van deze bevindingen (qPCR, Western Blot).
De bevindingen van de beschreven experimenten zullen gevalideerd worden in experimenten met primaire MM en/of LPL cellen, waarbij de exacte experimentele strategie gestuurd zal worden door de bevindingen van het onderzoek met de cellijnen.
Omschrijving doel en beoogde resultaten
Onderzoeksdoel: evaluatie van de therapeutische potentie van Trafinib als nieuwe ‘targeted therapy’ voor MM en LPL.
Beoogde resultaten: door uitgebreide in vitro analyses zal dit project de functionele en moleculaire effecten van Trafinib gemedieerde remming van CD40 in MM en LPL cellen in kaart brengen. Op basis van deze data kunnen vervolgstudies worden ontworpen om Trafinib verder te ontwikkelen als nieuwe behandeling voor MM en LPL.


